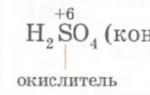Драгоценный металл - иридий. Металл иридий: история, свойства, как получают и где используют
Иридий металл выпадает в осадок после растворения платины в серной кислоте. После реакции металл становится черного цвета. Однако, его название переводят как «радуга». Дело в том, что соли иридия – это кладезь красок. Соединения с хлором – коричневые; с фтором – желтые; с бромом – синие. Вот и получил элемент имя греческой богини Ириды, а она, как известно, повелевала радугой.
Открыл металл-хамелеон Смитсон Теннат. Сделал это англичанин в 1804-ом году. Из того, что осадок иридия остается после реакции платины с концентрированной кислотой, следует, что радужный элемент практически непобедим. Растворяют его только перекись натрия и расплавленная щелочь.
Уникальны не только свойства иридия , редок и он сам. Геологи предполагают, что в недрах Земли его всего одна десятимиллиардная доля. Одна унция, а это всего около 30-ти граммов, стоит больше, тысячи долларов. Источником иридия служит не только платина, но и медно-никелевые руды. Правда, и в них содержание редкого металла ничтожно.
 Столь малую концентрацию иридия в земной коре ученые объясняют его внеземным происхождением. Считается, что иридий принесли метеориты и астероиды, упавшие на планету за все время ее существования. Иначе, замечают специалисты, тяжелых металлов (к каковым относится и иридий) вовсе не должно быть в земной коре. При образовании планеты все тяжелые элементы осели в ядре. Оно находится под таким давлением, что никакие силы не могут выбросить хоть грамм центра Земли на ее поверхность. Вывод, замечают ученые, напрашивается сам собой. Тем более, что наличие иридия в метеоритах
– факт зафиксированный.
Столь малую концентрацию иридия в земной коре ученые объясняют его внеземным происхождением. Считается, что иридий принесли метеориты и астероиды, упавшие на планету за все время ее существования. Иначе, замечают специалисты, тяжелых металлов (к каковым относится и иридий) вовсе не должно быть в земной коре. При образовании планеты все тяжелые элементы осели в ядре. Оно находится под таким давлением, что никакие силы не могут выбросить хоть грамм центра Земли на ее поверхность. Вывод, замечают ученые, напрашивается сам собой. Тем более, что наличие иридия в метеоритах
– факт зафиксированный.
По слоям земной коры, в которых высока концентрация радужного металла, геологи даже делают выводы о силе «космической атаки» на Землю в тот или иной период ее существования. Иридий космический, но нужен для вполне земных дел. Из него, к примеру, делают формы для выращивания кристаллов. В таких резервуарах можно получить любой камень, ведь элемент, как указывалось, не вступает в 99% химических реакций. То есть, формы из иридия совершенно «равнодушны» к растворам, помещенным в них.
 Не обходится без элемента и производство техники. Электрические контакты изготавливают именно из сплава иридия
и платины. Кстати, топливные баки для космических кораблей тоже сделаны из сплава на основе радужного элемента. В автомобилях же, иридий применяют в свечах зажигания.
Не обходится без элемента и производство техники. Электрические контакты изготавливают именно из сплава иридия
и платины. Кстати, топливные баки для космических кораблей тоже сделаны из сплава на основе радужного элемента. В автомобилях же, иридий применяют в свечах зажигания.
Электроды из редкого металла нашли применение и в медицине. Врачи выяснили, что если вживить электроды в головной мозг человека, можно излечить его от целого списка болезней. Главное, правильно рассчитать частоту сигнала, подаваемого на элементы. Болезнь Паркинсона лечит электрический сигнал в 25 Гц. Большая частота облегчает симптомы шизофрении и эпилепсии.
На слуху словосочетание «радиоактивный иридий ». Изотопы элемента используют при облучении больных раком, дабы остановить разрастание тканей. Чаще всего, редкий металл помещают в ампулу и вживляют в «тело» опухоли.
 Из иридия изготавливают глазные протезы, добавляют металл в аппараты для улучшения слуха. Иридиевые покрытия
спасают другие металлы от коррозии. Ей металл не подвержен даже при температуре в 2 тысячи градусов Цельсия. Но, наносить защитный слой обязательно электролитическим путем. Иначе, держаться на основе защитный слой не будет.
Из иридия изготавливают глазные протезы, добавляют металл в аппараты для улучшения слуха. Иридиевые покрытия
спасают другие металлы от коррозии. Ей металл не подвержен даже при температуре в 2 тысячи градусов Цельсия. Но, наносить защитный слой обязательно электролитическим путем. Иначе, держаться на основе защитный слой не будет.
Если знать, что в перьевых и шариковых ручках тоже используют иридий, становится понятно, почему некоторые экземпляры письменных принадлежностей столько стоят. Цену им добавляют не только известные фирмы-производители, но и шарики из редкого элемента на концах перьев или чернильных стержней.
Из сплава иридия с платиной делают некоторые инструменты для хирургии. Им нет сноса, как и украшениям, «родившимся» из тандема платины и радужного металла. Элемент №77 (таково его положение в таблице Менделеева) в ювелирные изделия из платины потому и добавляют, что без иридия она слишком мягка, не держит форму. Кольцо или серьга из чистой платины сомнется даже от легкого нажатия.
Правда, изделия, в составе которых есть иридий, дорогостоящие. Не только потому, что голубовато-серебристый металл уже причислили к драгоценным, но и потому что плавится он при температуре в несколько тысяч градусов. То есть получить сплав иридия с чем-либо не так-то просто. Нужна специальная и весьма недешевая аппаратура. Вот и выходит, что за небольшое иридиевое кольцо без каких-либо камней просят в среднем около 3 тысяч долларов.

Поставщиками металла №77 на мировой рынок являются: — Канада, Россия, ЮАР. В недрах последней страны иридия, как и платиновых и золотоносных залежей, больше всего. При общих запасах иридия в 15 тысяч тонн, в землях ЮАР скрываются 10 тысяч из них. Так, в 2009-ом году мировое производство редкого металла снизилось сразу на 13%. Все потому, что из-за внутренних проблем, элемент стали меньше добывать в Южно-Африканской республике. Ощутился дефицит иридия, цены на него подскочили. Так что, хоть ЮАР и развивающаяся страна, но без нее не могут развиваться и другие государства.
Среди предприятий, лидером в производстве иридия признана компания Lonmin. Она выпускает на рынок треть от общемировых объемов этого металла. Остается, надеется, что метеориты продолжат падать на землю, да так чтобы не нанести вреда людям. Иначе, вред им нанесет истощение запасов не только редкого, но и крайне, нужного человечеству металла.
Из чистого иридия делают тигли для лабораторных целей и мундштуки для выдувания тугоплавкого стекла. Можно, конечно, использовать и в качестве покрытия. Однако здесь встречаются трудности. Обычным электролитическим способом на другой металл наносится с трудом, и покрытие получается довольно рыхлое. Наилучшим электролитом был бы комплексный гексахлорид иридия, однако он неустойчив в водном растворе, и даже в этом случае качество покрытия оставляет желать лучшего.
Разработан метод получения иридиевых покрытий электролитическим путем из расплавленных цианидов калия и натрия при 600° С. В этом случае образуется плотное покрытие толщиной до 0,08 мм.
Менее трудоемко получение иридиевых покрытий методом плакирования. На основной металл укладывают тонкий слой металла-покрытия, а затем этот «бутерброд» идет под горячий пресс. Таким образом получают вольфрамовую и молибденовую проволоку с иридиевым покрытием. Заготовку из молибдена или вольфрама вставляют в иридиевую трубку и проковывают в горячем состоянии, а затем волочат до нужной толщины при 500-600° С. Эту проволоку используют для изготовления управляющих сеток в электронных лампах.
Можно наносить иридиевые покрытия на и керамику химическим способом. Для этого получают раствор комплексной соли иридия, например с фенолом или каким-либо другим органическим веществом. Такой раствор наносят на поверхность изделия, которое затем нагревают до 350-400° С в контролируемой атмосфере, т. е. в атмосфере с регулируемым окислительно-восстановительным потенциалом. Органика в этих условиях улетучивается, или выгорает, а слой иридия остается на изделии.
Но покрытия - не главное применение иридия. Этот металл улучшает механические и физико-химические свойства других металлов. Обычно его используют, чтобы повысить их прочность и твердость. Добавка 10% иридия к относительно мягкой платине повышает ее твердость и предел прочности почти втрое. Если же количество иридия в сплаве увеличить до 30%, твердость сплава возрастет ненамного, но зато предел прочности увеличится еще вдвое -до 99 кг/мм 2 . Поскольку такие обладают исключительной коррозионной стойкостью, из них делают жаростойкие тигли, выдерживающие сильный нагрев в агрессивных средах. В таких тиглях выращивают, в частности, кристаллы для лазерной техники. Платино-иридиевые привлекают и ювелиров - украшения из этих сплавов красивы и почти не изнашиваются. Из пла-тино-иридиевого сплава делают также эталоны, иногда - хирургический инструмент.
В будущем иридия с платиной могут приобрести особое значение в так называемой слаботочной технике как идеальный материал для контактов. Каждый раз, когда происходит замыкание и размыкание обычного медного контакта, возникает искра; в результате поверхность меди довольно быстро окисляется. В контакторах для сильных токов, например для электродвигателей, это явление не очень вредит работе: поверхность контактов время от времени зачищают наждачной бумагой, и контактор вновь готов к работе. Но, когда мы имеем дело со слаботочной аппаратурой, например в технике связи, тонкий слой окиси меди весьма сильно влияет на всю систему, затрудняет прохождение тока через контакт. А именно в этих устройствах частота включений бывает особенно большой - достаточно вспомнить АТС (автоматические телефонные станции). Вот здесь-то и придут на помощь необгорающие платино-иридиевые контакты - они могут работать практически вечно! Жаль только, что эти сплавы очень дороги и пока их недостаточно.
Добавляют не только к платине. Небольшие до-бавки элемента № 77 к вольфраму и молибдену увеличивают прочность этих металлов при высокой температуре. Мизерная добавка иридия к титану (0,1%) резко повышает его и без того значительную стойкость к действию кислот. же относится и к хрому. Термопары, состоящие из иридия и сплава иридия с родием (40% родия), надежно работают при высокой температуре в окислительной атмосфере. Из сплава иридия с осмием делают напайки для перьев авторучек и компасные иглы.
Резюмируя, можно сказать, что металлический иридий применяют главным образом из-за его постоянства - постоянны размеры изделий из металла, его физические и химические свойства, причем, если можно так выразиться, постоянны на высшем уровне.
Как и другие VIII группы, иридий может быть использован в химической промышленности в качестве катализатора. Иридиево-никелевые катализаторы иногда применяют для получения пропилена из ацетилена и метана. Иридий входил в состав платиновых катализаторов реакции образования окислов азота (в процессе получения азотной кислоты). Один из окислов иридия, IrO 2 , пытались применять в фарфоровой промышленности в качестве черной краски. Но слишком уж дорога эта краска…
Запасы иридия на Земле невелики, его содержание в земной коре исчисляется миллионными долями процента. Невелико и производство этого элемента - не больше тонны в год. Во всем мире!
В связи с этим трудно предположить, что со временем в судьбе иридия наступят разительные перемены - он навсегда останется редким и дорогим металлом. Но там, где его применяют, он служит безотказно, и в этой уникальной надежности залог того, что наука и промышленность будущего без иридия не обойдутся.
ИРИДИЕВЫЙ СТОРОЖ. Во многих химических и металлургических производствах, например в доменном, очень важно знать уровень твердых материалов в агрегатах. Обычно для такого контроля используют громоздкие зонды, подвешиваемые на специальных зондовых лебедках. В последние годы зонды стали заменять малогабаритными контейнерами с искусственным радиоактивным изотопом - иридием-192. Ядра 192 Ir испускают гамма-лучи высокой
энергии; период полураспада изотопа равен 74.4 суток, часть гамма-лучей поглощается шихтой, и приемники излучения фиксируют ослабление потока. Последнее пропорционально расстоянию,
которое проходят лучи в шихте. Иридий-192 с успехом применяют и для контроля сварных швов; с его помощью на фотопленке четко фиксируются все непроваренные места и инородные включения. Гамма-дефектоскопы с иридием-192 используют также для контроля качества изделий из стали и алюминиевых сплавов.
ЭФФЕКТ МЁССБАУЭРА. В 1958 г. молодой физик из Германии Рудольф
Мёссбауэр сделал открытие, обратившее на себя внимание всех физиков мира. Открытый Мёссбауэром эффект позволил с поразительной точностью измерять очень слабые ядерные явления. Через три года после открытия, в 1961 г., Мёссбауэр получил за свою работу Нобелевскую премию. Впервые этот эффект обнаружен на ядрах изотопа иридий-192.
БЬЕТСЯ АКТИВНЕЕ. Одно из наиболее интересных при менений платино-иридиевых сплавов за последние годы - изготовление из них электрических стимуляторов сердечной деятельности. В больного стенокардией вживляют электроды с пла-тино-иридиевыми зажимами. Электроды соединены с приемником, который тоже находится в теле больного. Генератор же с кольцевой антенной находится снаружи, например в кармане больного. Кольцевая антенна крепится на теле напротив приемника. Когда больной чувствует, что наступает приступ стенокардии, он включает генератор. В кольцевую антенну поступают импульсы, которые передаются в приемник, а от него - на платино-иридисвые электроды. Электроды, передавая импульсы на нервы, заставляют биться активнее.
СТАБИЛЬНЫЕ И НЕСТАБИЛЬНЫЕ. В предыдущих заметках довольно много говорилось о радиоизотопе иридий-192, применяемом в многочисленных приборах и даже причастном к важному научному открытию. Но, кроме иридия-192, у этого элемента есть еще 14 радиоактивных изотопов с массовыми числами от 182 до 198. Самый тяжелый изотоп в же время - самый ко-роткоживущий, его период полураспада меньше минуты. Изотоп иридий-183 интересен лишь тем, что его период полураспада - ровно один час. Стабильных же изотопов у иридия всего два. На долю более тяжелого - иридия-193 в природной смеси приходится 62,7%. Доля легкого иридия-191 соответственно 37,3%.
Химия
Больше двух столетий прошло с тех пор, как появились первые сведения о платине - белом металле из Южной Америки. Долгое время люди были уверены, что это чистый металл, так же, как золото. Только в самом начале XIX в. Волластон сумел выделить из самородной платины палладий и родий, а в 1804 г. Теннант, изучая черный осадок, оставшийся после растворения самородной платины в царской водке, нашел в нем еще два элемента. Один из них он назвал осмием , а второй - иридием. Соли этого элемента в разных условиях окрашивались в различные цвета. Это свойство и было положено в основу названия: по-гречески значит «радуга».
В 1841 г. известный русский химик профессор Карл Карлович Клаус занялся исследованием так называемых платиновых остатков, т. е. нерастворимого осадка, остающегося после обработки сырой платины царской водкой.
«При самом начале работы, - писал Клаус, - я был удивлен богатством моего остатка, ибо извлек из него, кроме 10% платины, немалое количество иридия, родия, осмия, несколько палладия и смесь различных металлов особенного содержания»...
Клаус сообщил горному начальству о богатстве остатков. Власти заинтересовались открытием казанского ученого, которое сулило значительные выгоды. Из платины в то время чеканили монету, и получение драгоценного металла из остатков казалось очень перспективным. Через год Петербургский монетный двор выделил Клаусу полпуда остатков. Но они оказались бедными платиной, и ученый решил провести на них исследование, «интересное для науки».
«Два года,- писал Клаус,- занимался я постоянно этим трудным, продолжительным и даже вредным для здоровья исследованием» и в 1845 г. опубликовал работу «Химическое исследование остатков уральской платиновой руды и металла рутения». Это было первое систематическое исследование свойств аналогов платины. В нем впервые были описаны и химические свойства иридия.
Клаус отмечал, что иридием он занимался больше, чем другими металлами платиновой группы. В главе об иридии он обратил внимание на неточности, допущенные Берцелиусом при определении основных констант этого элемента, и объяснил эти неточности тем, что маститый ученый работал с иридием, содержащим примесь рутения, тогда еще не известного химикам и открытого лишь в ходе «химического исследования остатков уральской платиновой руды и металла рутения».
Какой же он, иридий?
Атомная масса элемента № 77 равна 192,2. В таблице Менделеева он находится между осмием и платиной. И в природе он встречается главным образом в виде осмистого иридия - частого спутника самородной платины. Самородного иридия в природе нет.
Иридий - серебристо-белый металл
, очень твердый, тяжелый и прочный. По данным фирмы «Интернейшнл Никель и Ко», это самый тяжелый элемент: его плотность 22,65 г/см 3 , а плотность его постоянного спутника - осмия, второго по тяжести 22,61 г/см 3 . Правда, большинство исследователей придерживаются иной точки зрения: они считают, что иридий все-таки немного легче осмия.
Естественное свойство иридия (он же платиноид!) - высокая коррозионная стойкость. На него не действуют кислоты ни при нормальной, ни при повышенной температуре. Даже знаменитой царской водке монолитный иридий «не по зубам». Только расплавленные щелочи и перекись натрия вызывают окисление элемента № 77.
Иридий стоек к действию галогенов. Он реагирует с ними с большим трудом и только при повышенной температуре. Хлор образует с иридием четыре хлорида: IrCl, IrCl 2 , IrСl 3 и 1гСl 4 . Треххлористый иридий получается легче всего из порошка иридия, помещенного в струю хлора при 600° С. Единственное галоидное соединение, в котором иридий шестивалентен,- это фторид IrF 6 . Тонкоизмельченный иридий окисляется при 1000° С и в струе кислорода, причем в зависимости от условий могут получаться несколько соединений разного состава.
Как и все металлы платиновой группы, иридий образует комплексные соли. Среди них есть и соли с комплексными катионами, например Сl 3 и соли с комплексными анионами, например К 3 *ЗН 2 0. Как комплексообразователь иридий похож на своих соседей по таблице Менделеева.
Чистый иридий получают из самородного осмистого иридия и из остатков платиновых руд (после того как из них извлечены платина , осмий, палладий и рутений). О технологии получения иридия распространяться не будем, отослав читателя к статьям «Родий», «Осмий» и «Платина».
Иридий получают в виде порошка, который затем прессуют в полуфабрикаты и сплавляют или же порошок переплавляют в электрических печах в атмосфере аргона. Чистый иридий в горячем состоянии можно ковать, однако при обычной температуре он хрупок и не поддается никакой обработке.
Иридий в деле
Из чистого иридия делают тигли для лабораторных целей и мундштуки для выдувания тугоплавкого стекла. Можно, конечно, использовать иридий и в качестве покрытия. Однако здесь встречаются трудности. Обычным электролитическим способом иридий на другой металл наносится с трудом, и покрытие получается довольно рыхлое. Наилучшим электролитом был бы комплексный гексахлорид иридия, однако он неустойчив в водном растворе, и даже в этом случае качество покрытия оставляет желать лучшего.
Разработан метод получения иридиевых покрытий электролитическим путем из расплавленных цианидов калия и натрия при 600° С. В этом случае образуется плотное покрытие толщиной до 0,08 мм.
Менее трудоемко получение иридиевых покрытий методом плакирования. На основной металл укладывают тонкий слой металлапокрытия, а затем этот «бутерброд» идет под горячий пресс. Таким образом получают вольфрамовую и молибденовую проволоку с иридиевым покрытием. Заготовку из молибдена или вольфрама вставляют в иридиевую трубку и проковывают в горячем состоянии, а затем волочат до нужной толщины при 500-600° С. Эту проволоку используют для изготовления управляющих сеток в электронных лампах.
Можно наносить иридиевые покрытия на металлы и керамику химическим способом. Для этого получают раствор комплексной соли иридия, например с фенолом или каким-либо другим органическим веществом. Такой раствор наносят на поверхность изделия, которое затем нагревают до 350-400° С в контролируемой атмосфере, т. е. в атмосфере с регулируемым окислительно-восстановительным потенциалом. Органика в этих условиях улетучивается, или выгорает, а слой иридия остается на изделии.
Но покрытия - не главное применение иридия. Этот металл улучшает механические и физико-химические свойства других металлов. Обычно его используют, чтобы повысить их прочность и твердость. Добавка 10% иридия к относительно мягкой платине повышает ее твердость и предел прочности почти втрое. Если же количество иридия в сплаве увеличить до 30%, твердость сплава возрастет ненамного, но зато предел прочности увеличится еще вдвое - до 99 кг/мм 2 . Поскольку такие сплавы обладают исключительной коррозионной стойкостью, из них делают жаростойкие тигли, выдерживающие сильный нагрев в агрессивных средах. В таких тиглях выращивают, в частности, кристаллы для лазерной техники. Платино-иридиевые сплавы привлекают и ювелиров - украшения из этих сплавов красивы и почти не изнашиваются. Из платино-иридиевого сплава делают также эталоны, иногда - хирургический инструмент.
В будущем сплавы иридия с платиной могут приобрести особое значение в так называемой слаботочной технике как идеальный материал для контактов. Каждый раз, когда происходит замыкание и размыкание обычного медного контакта, возникает искра; в результате поверхность меди довольно быстро окисляется. В контакторах для сильных токов, например для электродвигателей, это явление не очень вредит работе: поверхность контактов время от времени зачищают наждачной бумагой, и контактор вновь готов к работе. Но, когда мы имеем дело со слаботочной аппаратурой, например в технике связи, тонкий слой окиси меди весьма сильно влияет на всю систему, затрудняет прохождение тока через контакт. А именно в этих устройствах частота включений бывает особенно большой - достаточно вспомнить АТС (автоматические телефонные станции). Вот здесь-то и придут на помощь не обгорающие платино-иридиевые контакты - они могут работать практически вечно! Жаль только, что эти сплавы очень дороги и пока их недостаточно.
Добавляют не только к платине. Небольшие добавки элемента № 77 к вольфраму и молибдену увеличивают прочность этих металлов при высокой температуре. Мизерная добавка иридия к титану (0,1%) резко повышает его и без того значительную стойкость к действию кислот. То же относится и к хрому. Термопары, состоящие из иридия и сплава иридия с родием (40% родня), надежно работают при высокой температуре в окислительной атмосфере. Из сплава иридия с осмием делают напайки для перьев авторучек и компасные иглы.
Резюмируя, можно сказать, что металлический иридий применяют из-за его постоянства. Как и другие металлы VIII группы, иридий может быть использован в химической промышленности в качестве катализатора. Иридиево-никелевые катализаторы иногда применяют для получения пропилена из ацетилена и метана. Иридий входил в состав платиновых катализаторов реакции образования окислов азота (в процессе получения азотной кислоты).. Один из окислов иридия, Ir0 2 , пытались применять в фарфоровой промышленности в качестве черной краски. Но слишком уж дорога эта краска...
Запасы иридия на Земле невелики, его содержание в земной коре исчисляется миллионными долями процента. Невелико и производство этого элемента - не больше тонны в год. Во всем мире! В связи с этим трудно предположить, что со временем в судьбе иридия наступят разительные перемены - он навсегда останется редким и дорогим металлом. Но там, где его применяют, он служит безотказно, и в этой уникальной надежности залог того, что наука и промышленность будущего без иридия не обойдутся.
ИРИДИЕВЫЙ СТОРОЖ. Во многих химических и металлургических производствах, например в доменном, очень важно знать уровень твердых материалов в агрегатах. Обычно для такого контроля используют громоздкие зонды, подвешиваемые на специальных зондовых лебедках. В. последние годы зонды стали заменять малогабаритными контейнерами с искусственным радиоактивным изотопом - иридием-192. Ядра 1921г испускают гамма-лучи высокой энергий; период полураспада изотопа равен 74,4 суток. Часть гамма-лучей поглощается шихтой, и приемники излучения фиксируют ослабление потока. Последнее пропорционально расстоянию, которое проходят лучи в шихте. Иридий-192 с успехом применяют и для контроля сварных швов; с его помощью на фотопленке четко фиксируются все непроваренные места и инородные включения. Гамма-дефектоскопы с иридием-192 используют также для контроля качества изделий из стали и алюминиевых сплавов.
ЭФФЕКТ МЁССБАУЭРА. В 1958 г. молодой физик из ФРГ Рудольф Мёссбауэр сделал открытие, обратившее на себя внимание всех физиков мира. Открытый Мёссбауэром эффект позволил с поразительной точностью измерять очень слабые ядерные явления. Через три года после открытия, в 1961 г., Мёссбауэр получил за свою работу Нобелевскую премию. Впервые этот эффект обнаружен на ядрах изотопа иридий-192.
СЕРДЦЕ БЬЕТСЯ АКТИВНЕЕ. Одно из наиболее интересных применений платино-иридиевых сплавов за последние годы - изготовление из них электрических стимуляторов сердечной деятельности. В сердце больного стенокардией вживляют электроды с платино-иридиевыми зажимами. Электроды соединены с приемником, который тоже находится в теле больного. Генератор же с кольцевой антенной находится снаружи, например в кармане больного. Кольцевая антенна крепится на теле напротив приемника. Когда больной чувствует, что наступает приступ стенокардии, он включает генератор. В кольцевую антенну поступают импульсы, которые передаются в приемник, а от него - на платино-иридиевые электроды. Электроды, передавая импульсы на нервы, заставляют сердце биться активнее. Сейчас в России многие станции скорой помощи оборудованы подобными генераторами. В случае остановки сердца делают надрез ключичной вены, вводят в нее соединенный с генератором электрод, включают генератор, и через несколько минут сердце вновь начинает работать.
ИЗОТОПЫ-СТАБИЛЬНЫЕ И НЕСТАБИЛЬНЫЕ. В предыдущих заметках довольно много говорилось о радиоизотопе иридий-192, применяемом в многочисленных приборах и даже причастном к важному научному открытию. Но, кроме иридия-192, у этого элемента есть еще 14 радиоактивных изотопов с массовыми числами от 182 до 198. Самый тяжелый изотоп в то же время - самый короткоживущий, его период полураспада меньше минуты. Изотоп иридий-183 интересен лишь тем, что его период полураспада - ровно один час. Стабильных же изотопов у иридия всего два. На долю более тяжелого - иридия-193 в природной смеси приходится 62,7%. Доля легкого иридия-191 соответственно 37,3%.
ПОЛЕЗНЫЕ ХЛОРИРИДАТЫ. Хлориридатами называют комплексные хлориды четырехвалентного иридия; общая их формула Ме 2 . Благодаря хлориридатам можно в принципе уверенно разделять соединения таких похожих элементов, как натрий и калий. Хлориридат натрия растворим в воде, а хлориридат калия - практически нерастворим. Но для такой операции хлориридаты слишком дороги, так как дорог исходный иридий. Это не значит однако, что хлориридаты вообще бесполезны. Способность иридия образовывать эти соединения используют для выделения элемента № 77 из смеси платиновых металлов.

Железоникелевый метеорит, содержавший в себе немало иридия и прочих , а потому чрезвычайно массивный, врезался в Землю, ударив по краю полуострова Юкатан (Мексика) 65 млн. лет назад – в эпоху безраздельного царствования динозавров.
Грунт из кратера диаметром в 180 и глубиной в 20 километров частью испарился (вместе с большей частью иридия), частью распылился. Наступили пыльные сумерки. Ударной волной, прошедшей как сквозь, так и вокруг планеты, были инициированы масштабные извержения в Азии и на территории Индостана, в ту пору плывшего от Мадагаскара на север и еще даже не пересекшего экватора. Дым и пыль вулканического происхождения усугубили ситуацию еще более...
Иридий – маркер космической катастрофы
Некоторые из ученых высказывают гипотезу, что динозавров погубило обилие тяжелых металлов в воздушной взвеси. Однако наиболее передовые биологи склонны считать фатальным стечение двух факторов: колоссальных размеров животных и...чихательного рефлекса. Резкое повышение артериального давления при спонтанном прочищении дыхательных путей губительно для кровеносных сосудов – особенно если чихать приходится непрестанно.Исчезновение динозавров дало возможность развития млекопитающим, итогом эволюции которых стало появление человека. Благодарный небесному заступничеству, человек провел исследования метеоритных остатков из наиболее крупных кратеров. Содержание иридия в обломках металлических гостей из космоса оказалось рекордным. Столь же рекордно содержание иридия в осадочных породах, укрывших землю вскоре после юкатанской катастрофы.
Однако больше всего благородного металла, уверены геологи, скрыто в недрах Земли.
Происхождение и свойства иридия
Как и все платиноиды, иридий – продукт многоступенчатого ядерного синтеза элементов , возможного при взрывах сверхновых или в катаклизмах еще большего масштаба. Образуется иридия немного, но Земле повезло формироваться в области, богатой металлами. Естественной (хотя и неподтвержденной) представляется концентрация иридия (равно как и , и платины) в ядре планеты.Остатки иридия в земной коре незначительны (золота в 40 раз больше), однако позволяют ежегодно добывать несколько тонн благородного металла. Честь открытия и наименования иридия принадлежит англичанину Смитсону Теннанту. Восхищенный разноцветьем солей металла (молочно-белый KIrF6, лимонно-желтый IrF5, желтый K3IrCl6, зеленый Na3IrBr6, бордовый Cs3IrI6, малиновый Na2IrBr6, черный IrI3), ученый предложил дать новому элементу имя Ириды – греческой богини радуги.

В обработке иридий неподатлив. Тридцать лет ушло на получение металла, очищенного от примесей. Как оказалось, беспримесный иридий ковок при температурах яркого свечения. Охлаждаясь, он утрачивает способность переносить механические воздействия и крошится под нагрузкой. Иридиевый порошок, запаянный в стеклянные сосуды – продукт работы аффинажных предприятий.
Долгое время иридий считался чемпионом по параметру плотности. Уже в наши дни теоретические расчеты вывели на первое место осмий – однако разница настолько невелика, что подтвердить ее простым взвешиванием не удается. Да и отделение осмия от иридия – задача непростая!
Иридий и осмий – братья навек
В природе иридий и осмий нередко объединяются . Естественная смесь металлов может называться осмиридий – если осмия больше – или иридиосмий, если процент иридия в сплаве выше. В отечественной минералогической практике закрепились названия осмирида и иридистого осмия.По легендам, в первой половине ХХ века обточенные кристаллики натурального осмирида припаивали к кончикам золотых перьев «вечных» ручек для обеспечения мягкости письма. На самом деле подобные опыты единичны, а в массовой реальности золотые перья авторучек упрочняют вольфрамом.

В среде любителей ювелирного искусства существует небольшой, но устойчивый и совершенно не удовлетворенный спрос на изделия из натурального осмирида. Любители экзотических украшений иногда спрашивают о возможности изготовления осмиридиевых изделий.
К сожалению, минерал этот крайне редок и не слишком декоративен – хотя и характеризуется сильным металлическим блеском. Осмирид тверд, хрупок и почти не поддается механической обработке. К тому же природная смесь иридия и осмия часто содержит немалое количество примесей – платины, золота, – что меняет и вид, и стоимость материала.
Искусственно полученные сплавы иридия и осмия строго нормированы по процентному составу элементов, но дороги, востребованы в промышленности и нетехнологичны в ювелирном отношении.
Применение иридия
После того, как выяснилась незаменимость иридия для производства свечей зажигания премиального качества, основным потребителем благородного металла стала автомобильная промышленность. Подъемы и спады в производстве легковых авто и иридиевых свечей для них обуславливают перепады цен на очищенный металл. За один год автостроители мира могут поднять спрос на иридий с одной тонны до почти одиннадцати – чтобы в следующем году, из-за кризисного снижения продаж, обойтись полутонной драгоценного платиноида.Потребность в иридии постоянна у изготовителей техники, работающей в экстремальных условиях. Реактивные двигатели нуждаются в иридиевых сплавах из-за их высокотемпературной прочности. Жаропрочный сплав иридия – элемент силовых установок космических роботов, работающих на атомной энергии. Сплавленный с иридием титан служит в трубопроводах, способных работать в океанских глубинах.
Радиоактивный иридий 192 – главный инструмент контроля качества сварных швов . Этот же источник гамма-излучения помогает врачам побеждать опухолевые процессы.
Слой иридия толщиной в несколько атомов покрывает зеркала телескопов, принимающих рентгеновское излучение. В прошлом при помощи платино-иридиевого покрытия продлевали срок службы замков артиллерийских орудий.
В ювелирной отрасли иридий используется для отделки и инкрустаций, хотя с недавних предпринимаются попытки изготовления иридиевых украшений. Куда более традиционно иридирование ювелирной платины: десятипроцентная добавка иридия делает изделие прочным, износоустойчивым, красивым.
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
|
|||||||
Иридий
Больше двух столетий прошло с тех пор, как появились первые сведения о платине белом металле из Южной Америки. Долгое время люди были уверены, что это чистый металл, так же, как золото. Только в самом начале XIX в. Волластон сумел выделить из самородной платины палладий и родий, а в 1804 г. Теннант, изучая черный осадок, оставшийся после растворения самородной платины в царской водке, нашел в нем еще два элемента. Один из них он назвал осмием, а второй иридием. Соли этого элемента в разных условиях окрашивались в различные цвета. Это свойство и было положено в основу названия: по-гречески слово ιρις, значит «радуга».
В 1841 г. известный русский химик профессор Карл Карлович Клаус занялся исследованием так называемых платиновых остатков, т.е. нерастворимого осадка, остающегося после обработки сырой платины царской водкой. «При самом начале работы, писал Клаус, я был удивлен богатством моего остатка, ибо извлек из него, кроме 10% платины, немалое количество иридия, родия, осмия, несколько палладия и смесь различных металлов особенного содержания»...
Клаус сообщил горному начальству о богатстве остатков. Власти заинтересовались открытием казанского ученого, которое сулило значительные выгоды. Из платины в то время чеканили монету, и получение драгоценного металла из остатков казалось очень перспективным. Через год Петербургский монетный двор выделил Клаусу полпуда остатков. Но они оказались бедными платиной, и ученый решил провести на них исследование, «интересное для науки».
«Два года, писал Клаус, занимался я постоянно этим трудным, продолжительным и даже вредным для здоровья исследованием» и в 1845 г. опубликовал работу «Химическое исследование остатков уральской платиновой руды и металла рутения». Это было первое систематическое исследование свойств аналогов платины. В нем впервые были описаны и химические свойства иридия.
Клаус отмечал, что иридием он занимался больше, чем другими металлами платиновой группы. В главе об иридии он обратил внимание на неточности, допущенные Берцелиусом при определении основных констант этого элемента, и объяснил эти неточности тем, что маститый ученый работал с иридием, содержащим примесь рутения, тогда еще не известного химикам и открытого лишь в ходе «химического исследования остатков уральской платиновой руды и металла рутения».
Какой же он, иридий?
Атомная масса элемента №77 равна 192,2. В таблице Менделеева он находится между осмием и платиной. И в природе он встречается главным образом в виде осмистого иридия частого спутника самородной платины. Самородного иридия в природе нет.
Иридий серебристо-белый металл, очень твердый, тяжелый и прочный. По данным фирмы «Интернейшнл Никель и Ко», это самый тяжелый элемент: его плотность 22,65 г/см 3 , а плотность его постоянного спутника осмия, второго по тяжести 22,61 г/см 3 . Правда, большинство исследователей придерживаются иной точки зрения: они считают, что иридий все-таки немного легче осмия.
Естественное свойство иридия (он же платиноид!) высокая коррозионная стойкость. На него не действуют кислоты ни при нормальной, ни при повышенной температуре. Даже знаменитой царской водке монолитный иридий «не по зубам». Только расплавленные щелочи и перекись натрия вызывают окисление элемента №77.
Иридий стоек к действию галогенов. Он реагирует с ними с большим трудом и только при повышенной температуре. Хлор образует с иридием четыре хлорида: IrCl, IrCl 2 , IrCl 3 и IrCl 4 . Треххлористый иридий получается легче всего из порошка иридия, помещенного в струю хлора при 600°C. Единственное галоидное соединение, в котором иридий шестивалентен, это фторид IrF 6 . Тонкоизмельченный иридий окисляется при 1000°C и в струе кислорода, причем в зависимости от условий могут получаться несколько соединений разного состава.
Как и все металлы платиновой группы, иридий образует комплексные соли. Среди них есть и соли с комплексными катионами, например Cl 3 и соли с комплексными анионами, например K 3 · 3H 2 O. Как комплексообразователь иридий похож на своих соседей по таблице Менделеева.
Иридий получают в виде порошка, который затем прессуют в полуфабрикаты и сплавляют или же порошок переплавляют в электрических печах в атмосфере аргона. Чистый иридий в горячем состоянии можно ковать, однако при обычной температуре он хрупок и не поддается никакой обработке.
Иридий в деле
Из чистого иридия делают тигли для лабораторных целей и мундштуки для выдувания тугоплавкого стекла. Можно, конечно, использовать иридий и в качестве покрытия. Однако здесь встречаются трудности. Обычным электролитическим способом иридий на другой металл наносится с трудом, и покрытие получается довольно рыхлое. Наилучшим электролитом был бы комплексный гексахлорид иридия, однако он неустойчив в водном растворе, и даже в этом случае качество покрытия оставляет желать лучшего.
Разработан метод получения иридиевых покрытий электролитическим путем из расплавленных цианидов калия и натрия при 600°C. В этом случае образуется плотное покрытие толщиной до 0,08 мм.
Менее трудоемко получение иридиевых покрытий методом плакирования. На основной металл укладывают тонкий слой металла-покрытия, а затем этот «бутерброд» идет под горячий пресс. Таким образом получают вольфрамовую и молибденовую проволоку с иридиевым покрытием. Заготовку из молибдена или вольфрама вставляют в иридиевую трубку и проковывают в горячем состоянии, а затем волочат до нужной толщины при 500...600°C. Эту проволоку используют для изготовления управляющих сеток в электронных лампах.
Можно наносить иридиевые покрытия на металлы и керамику химическим способом. Для этого получают раствор комплексной соли иридия, например с фенолом или каким-либо другим органическим веществом. Такой раствор наносят на поверхность изделия, которое затем нагревают до 350...400°C в контролируемой атмосфере, т.е. в атмосфере с регулируемым окислительно-восстановительным потенциалом. Органика в этих условиях улетучивается, или выгорает, а слой иридия остается на изделии.
Но покрытия не главное применение иридия. Этот металл улучшает механические и физико-химические свойства других металлов. Обычно его используют, чтобы повысить их прочность и твердость. Добавка 10% иридия к относительно мягкой платине повышает ее твердость и предел прочности почти втрое. Если же количество иридия в сплаве увеличить до 30%, твердость сплава возрастет ненамного, но зато предел прочности увеличится еще вдвое до 99 кг/мм 2 . Поскольку такие сплавы обладают исключительной коррозионной стойкостью, из них делают жаростойкие тигли, выдерживающие сильный нагрев в агрессивных средах. В таких тиглях выращивают, в частности, кристаллы для лазерной техники. Платино-иридиевые сплавы привлекают и ювелиров украшения из этих сплавов красивы и почти не изнашиваются. Из платино-иридиевого сплава делают также эталоны, иногда хирургический инструмент.
В будущем сплавы иридия с платиной могут приобрести особое значение в так называемой слаботочной технике как идеальный материал для контактов. Каждый раз, когда происходит замыкание и размыкание обычного медного контакта, возникает искра; в результате поверхность меди довольно быстро окисляется. В контакторах для сильных токов, например для электродвигателей, это явление не очень вредит работе: поверхность контактов время от времени зачищают наждачной бумагой, и контактор вновь готов к работе. Но, когда мы имеем дело со слаботочной аппаратурой, например в технике связи, тонкий слой окиси меди весьма сильно влияет на всю систему, затрудняет прохождение тока через контакт. А именно в этих устройствах частота включений бывает особенно большой достаточно вспомнить АТС (автоматические телефонные станции). Вот здесь-то и придут на помощь необгорающие платино-иридиевые контакты они могут работать практически вечно! Жаль только, что эти сплавы очень дороги и пока их недостаточно.
Иридий добавляют не только к платине. Небольшие добавки элемента №77 к вольфраму и молибдену увеличивают прочность этих металлов при высокой температуре. Мизерная добавка иридия к титану (0,1%) резко повышает его и без того значительную стойкость к действию кислот. То же относится и к хрому. Термопары, состоящие из иридия и сплава иридия с родием (40% родия), надежно работают при высокой температуре в окислительной атмосфере. Из сплава иридия с осмием делают напайки для перьев авторучек и компасные иглы.
Резюмируя, можно сказать, что металлический иридий применяют главным образом из-за его постоянства постоянны размеры изделий из металла, его физические и химические свойства, причем, если можно так выразиться, постоянны на высшем уровне.
Как и другие металлы VIII группы, иридий может быть использован в химической промышленности в качестве катализатора. Иридиево-никелевые катализаторы иногда применяют для получения пропилена из ацетилена и метана. Иридий входил в состав платиновых катализаторов реакции образования окислов азота (в процессе получения азотной кислоты). Один из окислов иридия, IrO 2 , пытались применять в фарфоровой промышленности в качестве черной краски. Но слишком уж дорога эта краска...
Запасы иридия на Земле невелики, его содержание в земной коре исчисляется миллионными долями процента. Невелико и производство этого элемента не больше тонны в год. Во всем мире!
В связи с этим трудно предположить, что со временем в судьбе иридия наступят разительные перемены он навсегда останется редким и дорогим металлом. Но там, где его применяют, он служит безотказно, и в этой уникальной надежности залог того, что наука и промышленность будущего без иридия не обойдутся.
Иридиевый сторож
Во многих химических и металлургических производствах, например в доменном, очень важно знать уровень твердых материалов в агрегатах. Обычно для такого контроля используют громоздкие зонды, подвешиваемые на специальных зондовых лебедках. В последние годы зонды стали заменять малогабаритными контейнерами с искусственным радиоактивным изотопом иридием-192. Ядра 192 Ir испускают гамма-лучи высокой энергии; период полураспада изотопа равен 74,4 суток. Часть гамма-лучей поглощается шихтой, и приемники излучения фиксируют ослабление потока. Последнее пропорционально расстоянию, которое проходят лучи в шихте. Иридий-192 с успехом применяют и для контроля сварных швов; с его помощью па фотопленке четко фиксируются все непроваренные места и инородные включения. Гамма-дефектоскопы с иридием-192 используют также для контроля качества изделий из стали и алюминиевых сплавов.
Эффект Мёссбауэра
В 1958 г. молодой физик из ФРГ Рудольф Мёссбауэр сделал открытие, обратившее на себя внимание всех физиков мира. Открытый Мёссбауэром эффект позволил с поразительной точностью измерять очень слабые ядерные явления. Через три года после открытия, в 1961 г., Мёссбауэр получил за свою работу Нобелевскую премию. Впервые этот эффект обнаружен на ядрах изотопа иридий-192.
Сердце бьется активнее
Одно из наиболее интересных применений платино-иридиевых сплавов за последние годы изготовление из них электрических стимуляторов сердечной деятельности. В сердце больного стенокардией вживляют электроды с платино-иридиевыми зажимами. Электроды соединены с приемником, который тоже находится в теле больного. Генератор же с кольцевой антенной находится снаружи, например в кармане больного. Кольцевая антенна крепится на теле напротив приемника. Когда больной чувствует, что наступает приступ стенокардии, он включает генератор. В кольцевую антенну поступают импульсы, которые передаются в приемник, а от него на платино-придиевые электроды. Электроды, передавая импульсы на нервы, заставляют сердце биться активнее. Сейчас в СССР многие станции скорой помощи оборудованы подобными генераторами. В случае остановки сердца делают надрез ключичной вены, вводят в нее соединенный с генератором электрод, включают генератор, и через несколько минут сердце вновь начинает работать.
Изотопы стабильные и нестабильные
В предыдущих заметках довольно много говорилось о радиоизотопе иридий-192, применяемом в многочисленных приборах и даже причастном к важному научному открытию. Но, кроме иридия-192, у этого элемента есть еще 14 радиоактивных изотопов с массовыми числами от 182 до 198. Самый тяжелый изотоп в то же время самый короткоживущий, его период полураспада меньше минуты. Изотоп иридий-183 интересен лишь тем, что его период полураспада ровно один час. Стабильных же изотопов у иридия всего два. На долю более тяжелого иридия-193 в природной смеси приходится 62,7%. Доля легкого иридия-191 соответственно 37,3%.
Полезные хлориридаты
Хлориридатами называют комплексные хлориды четырехвалентного иридия; общая их формула Me 2 . Благодаря хлориридатам можно в принципе уверенно разделять соединения таких похожих элементов, как натрий и калий. Хлориридат натрия растворим в воде, а хлориридат калия практически нерастворим. Но для такой операции хлориридаты слишком дороги, так как дорог исходный иридий. Это не значит однако, что хлориридаты вообще бесполезны. Способность иридия образовывать эти соединения используют для выделения элемента №77 из смеси платиновых металлов.