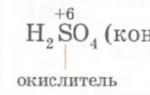Список солей и их названия. Соли: классификация и химические свойства
Определение солей в рамках теории диссоциации. Соли принято делить на три группы: средние, кислые и основные. В средних солях все атомы водорода соответствующей кислоты замещены на атомы металла, в кислых солях они замещены только частично, в основных солях группы ОН соответствующего основания частично замещены на кислотные остатки.
Существуют также некоторые другие типы солей, например двойные соли, в которых содержатся два разных катиона и один анион: СаСО 3 MgCO 3 (доломит), КСl NaCl (сильвинит), KAl(SO 4) 2 (алюмокалиевые квасцы); смешанные соли, в которых содержится один катион и два разных аниона: СаОСl 2 (или Са(ОСl)Сl); комплексные соли, в состав которых входит комплексный ион, состоящий из центрального атома, связанного с несколькими лигандами : K 4 (желтая кровяная соль), K 3 (красная кровяная соль), Na, Cl; гидратные соли (кристаллогидраты), в которых содержатся молекулы кристаллизационной воды: CuSO 4 5H 2 O(медный купорос), Na 2 SO 4 10Н 2 О (глауберова соль).
Название солей образуют из названия аниона, за которым следует название катиона.
Для солей бескислородных кислот к названию неметалла добавляют суффикс ид, например хлорид натрия NaCl, сульфид железа(Н) FeS и др.
При наименовании солей кислородсодержащих кислот к латинскому корню названия элемента добавляют в случае высших степеней окисления окончание — am , в случае низших степеней окисления окончание -ит. В названиях некоторых кислот для обозначения низших степеней окисления неметалла используют приставку гипо-, для солей хлорной и марганцовой кислот используют приставку пер-, например: карбонат кальция СаСО 3 , сульфат железа(III) Fe 2 (SO 4) 3 , сульфит железа(II) FeSO 3 , гипохлорит калия КОСl, хлорит калия КОСl 2 , хлорат калия КОСl 3 , перхлорат калия КОСl 4 , перманганат калия КМnO 4 , дихромат калия К 2 Сг 2 O 7 .
Кислые и основные соли можно рассматривать как продукт неполного превращения кислот и оснований. По международной номенклатуре атом водорода, входящий в состав кислой соли, обозначают приставкой гидро-, группу ОН - приставкой гидрокси, NaHS - гидросульфид натрия, NaHSO 3 - гидросульфит натрия, Mg(OH)Cl - гидроксихлорид магния, Аl(ОН) 2 Сl - дигидроксихлорид алюминия.
В названиях комплексных ионов сначала указывают лиганды, завершают названием металла с указанием соответствующей степени окисления (римскими цифрами в скобках). В названиях комплексных катионов используют русские названия металлов, например: Cl 2 - хлорид тетраамминмеди(П), 2 SO 4 - сульфат диамминсеребра(1). В названиях комплексных анионов используют латинские названия металлов с суффиксом -ат, например: К[Аl(ОН) 4 ] - тетрагидроксиалюминат калия, Na - тетра- гидроксихромат натрия, K 4 - гексацианоферрат(Н) калия.
Названия гидратных солеи (кристаллогридратов ) образуются двумя способами. Можно воспользоваться системой названий комплексных катионов, описанной выше; например, медный купорос SO 4 Н 2 0 (или CuSO 4 5Н 2 O) можно назвать сульфат тетрааквамеди(П). Однако для наиболее известных гидратных солей чаще всего число молекул воды (степень гидратации) указывают численной приставкой к слову «гидрат», например: CuSO 4 5Н 2 O - пентагидрат сульфата меди(И), Na 2 SO 4 10Н 2 О - декагидрат сульфата натрия, СаСl 2 2Н 2 O - дигидрат хлорида кальция.

Растворимость солей
По растворимости в воде соли делятся на растворимые (Р), нерастворимые (Н) и малорастворимые (М). Для определения растворимости солей пользуются таблицей растворимости кислот, оснований и солей в воде. Если таблицы под рукой нет, то можно воспользоваться правилами. Их легко запомнить.
1. Растворимы все соли азотной кислоты - нитраты.
2. Растворимы все соли соляной кислоты - хлориды, кроме AgCl (Н) , PbCl 2 (М) .
3. Растворимы все соли серной кислоты - сульфаты, кроме BaSO 4 (Н) , PbSO 4 (Н) .
4. Растворимы соли натрия и калия.
5. Не растворяются все фосфаты, карбонаты, силикаты и сульфиды, кроме солей Na + и K + .
Из всех химических соединений соли являются наиболее многочисленным классом веществ. Это твердые вещества, они отличаются друг от друга по цвету и растворимости в воде. В начале XIX в. шведский химик И. Берцелиус сформулировал определение солей как продуктов реакций кислот с основаниями или соединений, полученных заменой атомов водорода в кислоте металлом. По этому признаку различают соли средние, кислые и основные. Средние, или нормальные, соли - это продукты полного замещения атомов водорода в кислоте на металл.
Например:
Na 2 CO 3 - карбонат натрия;
CuSO 4 - сульфат меди (II) и т. д.
Диссоциируют такие соли на катионы металла и анионы кислотного остатка:
Na 2 CO 3 = 2Na + + CO 2 —
Кислые соли - это продукты неполного замещения атомов водорода в кислоте на металл. К кислым солям относят, например, питьевую соду NaHCO 3 , которая состоит из катиона металла Na + и кислотного однозарядного остатка HCO 3 — . Для кислой кальциевой соли формула записывается так: Ca(HCO 3) 2. Названия этих солей складываются из названий средних солей с прибавлением приставки гидро- , например:
Mg(HSO 4) 2 - гидросульфат магния.
Диссоциируют кислые соли следующим образом:
NaHCO 3 = Na + + HCO 3 —
Mg(HSO 4) 2 = Mg 2+ + 2HSO 4 —
Основные соли - это продукты неполного замещения гидроксогрупп в основании на кислотный остаток. Например, к таким солям относится знаменитый малахит (CuOH) 2 CO 3 , о котором вы читали в произведениях П. Бажова. Он состоит из двух основных катионов CuOH + и двухзарядного аниона кислотного остатка CO 3 2- . Катион CuOH + имеет заряд +1, поэтому в молекуле два таких катиона и один двухзарядный анион CO 3 2- объединены в электронейтральную соль.
Названия таких солей будут такими же, как и у нормальных солей, но с прибавлением приставки гидроксо- , (CuOH) 2 CO 3 - гидроксокарбонат меди (II) или AlOHCl 2 - гидроксохлорид алюминия. Большинство основных солей нерастворимы или малорастворимы.
Последние диссоциируют так:
AlOHCl 2 = AlOH 2 + + 2Cl —

Свойства солей


Первые две реакции обмена были подробно рассмотрены ранее.
Третья реакция также является реакцией обмена. Она протекает между растворами солей и сопровождается образованием осадка, например:

Четвертая реакция солей связана с положением металла в электрохимическом ряду напряжений металлов (см. «Электрохимический ряд напряжений металлов»). Каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений. Это соблюдается при выполнении следующих условий:
1) обе соли (и реагирующая, и образующаяся в результате реакции) должны быть растворимыми;
2) металлы не должны взаимодействовать с водой, поэтому металлы главных подгрупп I и II групп (для последней начиная с Са) не вытесняют другие металлы из растворов солей.


Способы получения солей
Способы получения и химические свойства солей. Соли могут быть получены из неорганических соединений практически любого класса. Наряду с этими способами соли бескислородных кислот могут быть получены при непосредственном взаимодействии металла и неметалла (Cl, S ит. д.).
Многие соли устойчивы при нагревании. Однако соли аммония, а также некоторые соли малоактивных металлов, слабых кислот и кислот, в которых элементы проявляют высшие или низшие степени окисления, при нагревании разлагаются.
СаСO 3 = СаО + СO 2
2Ag 2 CO 3 = 4Ag + 2СO 2 + O 2
NH 4 Cl = NH 3 + НСl
2KNO 3 = 2KNO 2 + O 2
2FeSO 4 = Fe 2 O 3 + SO 2 + SO 3
4FeSO 4 = 2Fe 2 O 3 + 4SO 2 + O 2
2Cu(NO 3) 2 = 2CuO + 4NO 2 + O 2
2AgNO 3 = 2Ag + 2NO 2 + O 2
NH 4 NO 3 = N 2 O + 2H 2 O
(NH 4) 2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4H 2 O
2КСlO 3 =MnO 2 = 2KCl + 3O 2
4KClO 3 = 3КСlO 4 + KCl
Основания могут взаимодействовать:
- с неметаллами -
6KOH + 3S → K2SO 3 + 2K 2 S + 3H 2 O;
- с кислотными оксидами -
2NaOH + CO 2 → Na 2 CO 3 + H 2 O;
- с солями (выпадение осадка, высвобождение газа) -
2KOH + FeCl 2 → Fe(OH) 2 + 2KCl.
Существую также другие способы получения:
- взаимодействие двух солей -
CuCl 2 + Na 2 S → 2NaCl + CuS↓;
- реакция металлов и неметаллов -
- соединение кислотных и основных оксидов -
SO 3 + Na 2 O → Na 2 SO 4 ;
- взаимодействие солей с металлами -
Fe + CuSO 4 → FeSO 4 + Cu.
Химические свойства
Растворимые соли являются электролитами и подвержены реакции диссоциации. При взаимодействии с водой они распадаются, т.е. диссоциируют на положительно и отрицательно заряженные ионы - катионы и анионы соответственно. Катионами являются ионы металлов, анионами - кислотные остатки. Примеры ионных уравнений:
- NaCl → Na + + Cl − ;
- Al 2 (SO 4) 3 → 2Al 3 + + 3SO 4 2− ;
- CaClBr → Ca2 + + Cl - + Br - .
Помимо катионов металлов в солях могут присутствовать катионы аммония (NH4 +) и фосфония (PH4 +).
Другие реакции описаны в таблице химических свойств солей.
Рис. 3. Выделение осадка при взаимодействии с основаниями.
Некоторые соли в зависимости от вида разлагаются при нагревании на оксид металла и кислотный остаток или на простые вещества. Например, СаСO 3 → СаO + СО 2 , 2AgCl → Ag + Cl 2 .
Что мы узнали?
Из урока 8 класса химии узнали об особенностях и видах солей. Сложные неорганические соединения состоят из металлов и кислотных остатков. Могут включать водород (кислые соли), два металла или два кислотных остатка. Это твёрдые кристаллические вещества, которые образуются в результате реакций кислот или щелочей с металлами. Реагируют с основаниями, кислотами, металлами, другими солями.
Солями называются сложные вещества, молекулы которых, состоят из атомов металлов и кислотных остатков (иногда могут содержать водород). Например, NaCl – хлорид натрия, СаSO 4 – сульфат кальция и т. д.
Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Na + Cl – – хлорид натрия
Ca 2+ SO 4 2– – сульфат кальция и т.д.
Соль является продуктом частичного или полного замещения металлом атомов водорода кислоты. Отсюда различают следующие виды солей:
1. Средние соли – все атомы водорода в кислоте замещены металлом: Na 2 CO 3 , KNO 3 и т.д.
2. Кислые соли – не все атомы водорода в кислоте замещены металлом. Разумеется, кислые соли могут образовывать только двух- или многоосновные кислоты. Одноосновные кислоты кислых солей давать не могут: NaHCO 3 , NaH 2 PO 4 ит. д.
3. Двойные соли – атомы водорода двух- или многоосновной кислоты замещены не одним металлом, а двумя различными: NaKCO 3 , KAl(SO 4) 2 и т.д.
4. Соли основные можно рассматривать как продукты неполного, или частичного, замещения гидроксильных групп оснований кислотными остатками: Аl(OH)SO 4 , Zn(OH)Cl и т.д.
По международной номенклатуре название соли каждой кислоты происходит от латинского названия элемента. Например, соли серной кислоты называются сульфатами: СаSO 4 – сульфат кальция, Mg SO 4 – сульфат магния и т.д.; соли соляной кислоты называются хлоридами: NaCl – хлорид натрия, ZnCI 2 – хлорид цинка и т.д.
В название солей двухосновных кислот добавляют частицу «би» или «гидро»: Mg(HCl 3) 2 – бикарбонат или гидрокарбонат магния.
При условии, что в трехосновной кислоте замещён на металл только один атом водорода, то добавляют приставку «дигидро»: NaH 2 PO 4 – дигидрофосфат натрия.
Соли – это твёрдые вещества, обладающие самой различной растворимостью в воде.
 Химические свойства солей
Химические свойства солей
Химические свойства солей определяются свойствами катионов и анионов, которые входят в их состав.
1. Некоторые соли разлагаются при прокаливании:
CaCO 3 = CaO + CO 2
2. Взаимодействуют с кислотами с образованием новой соли и новой кислоты. Для осуществление этой реакции необходимо, чтобы кислота была более сильная чем соль, на которую воздействует кислота:
2NaCl + H 2 SO 4 → Na 2 SO 4 + 2HCl.
3. Взаимодействуют с основаниями , образуя новую соль и новое основание:
Ba(OH) 2 + Mg SO 4 → BaSO 4 ↓ + Mg(OH) 2 .
4. Взаимодействуют друг с другом с образованием новых солей:
NaCl + AgNO 3 → AgCl + NaNO 3 .
5. Взаимодействуют с металлами, которые стоят в раду активности до металла, который входит в состав соли:
Fe + CuSO 4 → FeSO 4 + Cu↓.
Остались вопросы? Хотите знать больше о солях?
Чтобы получить помощь репетитора – .
Первый урок – бесплатно!
blog.сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
В таблице 15 приведены названия часто встречающихся кислот, их молекулярные и структурные формулы, а также формульные единицы и названия соответствующих солей.
Таблица помогает составлять химические формулы солей бескислородных и кислородсодержащих кислот. Для образования химических формул солей надо атомы водорода в кислотах заменить на атомы металлов с учётом их валентности.
Приведённые названия кислот и солей соответствуют принятой международной номенклатуре.
Название бескислородных кислот образуются по правилам для бинарных соединений.
Названия солей начинаются с названия кислотного остатка в именительном падеже. Это название образуется из корня латинского названия химического элемента, образующего кислоту, и окончания "ат" или "ит" в случае солей кислородсодержащих кислот, для солей бескислородных кислот – "ид". Затем в солях бескислородных кислот называется металл в родительном падеже. Причём если атом металла может иметь разную валентность, то её отмечают римской цифрой (в скобках) после названия химического элемента (без пробела). Например, хлорид железа(II) и хлорид олова(IV).
Включение в таблицу названий молекулярных и структурных формул часто встречающихся кислот позволяет легко запомнить приведённые в ней сведения.
Названия кислот типа H n XO m составляют с учётом валентности (степени окисления) центрального атома:
– атом X имеет высшую (или единственную) валентность (степень окисления): H 2 SО 4 – серная; HNО 3 – азотная; Н 2 СО 3 – угольная;
– атом X имеет промежуточные степени окисления: H 2 SO 3 – сернистая; HNО 2 – азотистая; НСlО – хлорноватистая.
Таблица 15
Составление химических формул солей
ГЕНЕТИЧЕСКАЯ СВЯЗЬ КЛАССОВ
НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Таблица 16 показывает в виде схемы взаимосвязь неорганических веществ разных классов. Изучение свойств веществ показывает, что можно при помощи химических реакций переходить от простых веществ к сложным и от одних сложных веществ к другим. Связь между веществами разных классов, основанная на их взаимопревращениях и отражающая единство их происхождения, называется генетической .
Вещества по составу подразделяются на простые и сложные. Среди простых веществ различают металлы и неметаллы. Эти две группы веществ могут образовывать многочисленные сложные вещества. К основным классам неорганических соединений принадлежат оксиды, гидроксиды и соли. Связь между этими классами веществ обозначена при помощи стрелок.
По таблице можно проследить переходы металлов и неметаллов в оксиды и гидроксиды:
Эти две цепочки превращений аналогичны и роднят металлы и неметаллы.
Однако надо подчеркнуть, что простое вещество металл является родоначальником сложных веществ, обладающих оснóвными свойствами (оснóвных оксидов и оснований). Простое вещество неметалл выступает в качестве родоначальника сложных веществ, проявляющих кислотные свойства (кислотных оксидов и кислот).
Различие свойств кислотных и оснóвных оксидов, а также свойств кислот и оснований приводит к их взаимодействию друг с другом с образованием солей. Таким образом, соли генетически связаны с исходными веществами – металлами и неметаллами – посредством их оксидов и гидроксидов.
Так как соли представляют собой продукты реакций кислот и оснований, то по составу различают средние (нормальные), кислые и оснóвные соли. Кислые соли содержат в своём составе атомы водорода, оснóвные – гидроксогруппы. Названия кислых солей складываются из названий солей с прибавлением слова "гидро", а основных – "гидроксо".
Существуют также двойные соли (соли двух металлов), к ним относят, например, алюмокалиевые квасцы KA1(SО 4) 2 · 12Н 2 О, смешанные соли NаСl · NаF, СаВrСl, комплексные соли Nа 2 , К 3 , К 4 , включая кристаллогидраты СuSО 4 · 5Н 2 О (медный купорос), Nа 2 SО 4 · 10Н 2 О (глауберова соль)
Необходимо научиться составлять химические формулы гидроксидов (кислородсодержащих кислот и оснований) для атома элемента Э с валентностью "n". Гидроксиды получают по реакции присоединения воды к соответствующим оксидам. При этом не имеет значение, происходит ли эта реакция в реальных условиях. Например, химическую формулу угольной кислоты получают сложением всех атомов по уравнению реакции
СО 2 + Н 2 О = Н 2 СО 3 .
Химические формулы метафосфорной , пирофосфорной и ортофосфорной кислот составляют из формулы оксида фосфора(V)1 и соответственно одной, двух и трёх молекул воды:
Р 2 О 5 + Н 2 О = 2НРО 3 ;
Р 2 О 5 + 2Н 2 О = Н 4 Р 2 О 7 ;
Р 2 О 5 + 3Н 2 О = 2Н 3 РО 4 .
Приведённая схема взаимосвязи между классами неорганических веществ не охватывает всего многообразия химических соединений. В этой схеме в качестве бинарных веществ выступают оксиды,
Таблица 16
Когда слышишь слово "соль", то первая ассоциация, конечно же, поваренная, без которой любое блюдо покажется невкусным. Но ведь это не единственное вещество, которое относится к классу химических веществ соли. Примеры, состав и химические свойства солей вы сможете найти в этой статье, а также научитесь правильно составлять название любой из них. Прежде чем продолжить, давайте договоримся, в этой статье мы рассмотрим только неорганические средние соли (полученные при реакции неорганических кислот с полным замещением водорода).
Определение и химический состав
Одно из определений соли звучит так:
- (т. е. состоящее из двух частей), в состав которого входят ионы металлов и кислотный остаток. То есть это вещество, получившееся в результате реакции кислоты и гидроксида (оксида) любого металла.
Есть еще одно определение:
- Это соединение, представляющее собой продукт полного или частичного замещения ионов водорода кислоты ионами металла (подходит для средних, основных и кислых).
Оба определение правильные, но не отражают всю суть процесса получения соли.
Классификация солей
Рассматривая различных представителей класса солей, можно заметить, что они бывают:
- Кислородсодержащими (соли серной, азотной, кремниевой и других кислот, в состав кислотного остатка которых входит кислород и еще один неметалл).
- Бескислородными, т. е. соли, образованные при реакции остаток которой не содержит кислород, — соляная, бромоводородная, сероводородная и другие.
По количеству замещенных водородов:
- Одноосновные: соляная, азотная, иодоводородная и другие. В состав кислоты входит один ион водорода.
- Двухосновные: два иона водорода замещены ионами металлов при образовании соли. Примеры: серная, сернистая, сероводородная и другие.
- Трехосновные: в составе кислоты три иона водорода замещены металлическими ионами: фосфорная.
Есть и другие типы классификаций по составу и свойствам, но мы не станем их разбирать, так как цель статьи немного другая.
Учимся называть правильно
У любого вещества есть название, которое понятно только жителям определенного региона, его еще называют тривиальным. Поваренная соль — пример разговорного названия, по международной номенклатуре оно будет называться уже по-другому. Но в разговоре абсолютно любой человек, знакомый с номенклатурой названий, без проблем поймет, что речь идет о веществе с химической формулой NaCl. Эта соль является производной от соляной кислоты, а соли ее называют хлоридами, то есть называется она хлорид натрия. Нужно просто выучить названия солей, приведенных ниже в таблице, а затем добавить название металла, образовавшего соль.
Но так просто составляется название, если у металла неизменная валентность. А теперь рассмотрим с названием), у которой металл с переменной валентностью — FeCl 3. Вещество называется хлорид железа трехвалентного. Именно такое название правильное!
| Формула кислоты | Название кислоты | Кислотный остаток (формула) | Номенклатурное название | Пример и тривиальное название |
| HCl | соляная | Cl - | хлорид | NaCl (поваренная соль, каменная соль) |
| HI | иодоводородная | I - | иодид | NaI |
| HF | фтороводородная | F - | фторид | NaF |
| HBr | бромоводородная | Br - | бромид | NaBr |
| H 2 SO 3 | сернистая | SO 3 2- | сульфит | Na 2 SO 3 |
| H 2 SO 4 | серная | SO 4 2- | сульфат | CaSO 4 (ангидрит) |
| HClO | хлорноватистая | ClO - | гипохлорит | NaClO |
| HClO 2 | хлористая | ClO 2 - | хлорит | NaClO 2 |
| HClO 3 | хлорноватая | ClO 3 - | хлорат | NaClO 3 |
| HClO 4 | хлорная | ClO 4 - | перхлорат | NaClO 4 |
| H 2 CO 3 | угольная | CO 3 2- | карбонат | CaCO 3 (известняк, мел, мрамор) |
| HNO 3 | азотная | NO 3 - | нитрат | AgNO 3 (ляпис) |
| HNO 2 | азотистая | NO 2 - | нитрит | KNO 2 |
| H 3 PO 4 | фосфорная | PO 4 3- | фосфат | AlPO 4 |
| H 2 SiO 3 | кремниевая | SiO 3 2- | силикат | Na 2 SiO 3 (жидкое стекло) |
| HMnO 4 | марганцовая | MnO 4 - | перманганат | KMnO 4 (марганцовка) |
| H 2 CrO 4 | хромовая | CrO 4 2- | хромат | CaCrO 4 |
| H 2 S | сероводородная | S- | сульфид | HgS (киноварь) |
Химические свойства
Как класс, соли по своим химическим свойствам характеризуются тем, что могут взаимодействовать со щелочами, кислотами, солями и более активными металлами:
1. При взаимодействии со щелочами в растворе обязательным условием реакции является выпадение в осадок одного из получаемых веществ.
2. При взаимодействии с кислотами реакция проходит, если образуется летучая кислота, нерастворимая кислота или нерастворимая соль. Примеры:
- К летучим кислотам относится угольная, так как она легко распадается на воду и углекислый газ: MgCO 3 + 2HCl = MgCl 2 + H 2 O + CO 2.
- Нерастворимая кислота — кремниевая, образуется в результате реакции силиката с другой кислотой.
- Одним из признаков химической реакции является выпадение осадка. Какие соли можно посмотреть в таблице растворимости.
3. Взаимодействие солей между собой происходит только в случае связывания ионов, т. е. одна из образовавшихся солей выпадает в осадок.
4. Чтобы определить, пойдет ли реакция между металлом и солью, нужно обратиться к таблице напряжения металлов (иногда ее еще называют рядом активности).

Только более активные металлы (расположенные левее) могут вытеснять из соли металл. Примером является реакция железного гвоздя с медным купоросом:
CuSO 4 + Fe= Cu + FeSO 4

Такие реакции свойственны большинству представителей класса солей. Но есть и более специфические реакции в химии, свойства соли индивидуальные отражающие, например разложение при накаливании или образование кристаллогидратов. Каждая соль индивидуальна и по-своему необычна.